安全性試験
臨床試験(治験)を安全に、安心して実施するため、また、労働者の安全担保やSDS作成のため、副作用や皮膚や眼に対する刺激性、アレルギー反応などがないか、リスクを評価いたします。
一般毒性試験
単回投与毒性試験/急性毒性試験/急性全身毒性試験
単回投与毒性試験
単回投与毒性試験
サンプルを臨床適用経路(経口、経皮、静脈内投与等)から1回投与し、一般状態、体重変化を14日間観察し、観察終了時には剖検(肉眼的観察)により評価いたします。追加で血液検査、病理組織学的検査も実施可能です。
‐試験日程例-

急性毒性試験
急性経口毒性試験-固定用量法(OECD TG420)
原則雌を用いて実施いたします。投与用量は5、50、300、2000mg/kg用量とし、先ずは見当付試験として1匹ずつ毒性状況を確認しながらフローチャートに従って進めます。次に死亡しない用量で4匹を用いた本試験を実施し、概略のLD50を求めます。事前の毒性情報がなければ300mg/kg用量からスタートいたします。検査方法は単回投与毒性試験と同様になります。
急性経口毒性試験-毒性等級法(OECD TG423)
原則雌を用いて実施いたします。投与用量は5、50、300、2000mg/kg用量とし、3匹ずつ毒性状況を確認しながらフローチャートに従って進め、概略のLD50を求めます。事前の毒性情報がなければ300mg/kg用量からスタートいたします。検査方法は単回投与毒性試験と同様になります。概略のLD50を求める場合はこちらをお勧めいたします。
急性経皮毒性試験(OECD TG402)
サンプルを1回背部に24時間閉塞貼布し、一般症状、体重変化を14日間観察します。観察終了時には剖検(肉眼的観察)により評価いたします。追加で病理組織学的検査も実施可能です。
急性吸入毒性試験(OECD TG403)
サンプルを1回(通常4-6時間)鼻部暴露し、一般症状、体重変化を14日間観察します。観察終了時には剖検(肉眼的観察)により評価いたします。追加で病理組織学的検査も実施可能です。
マウスを用いる簡易吸入試験
当該試験は、当社の規定容量のチャンバー内にマウスを収納し、ご指定量の被験検体を噴霧してその影響を記述する簡易的な試験方法です。比較的安価にサービスを提供させていただくことが可能ですが、実験動物を用いた一定条件下での非臨床研究データとなります。ヒト(あるいはペット)において、吸入毒性がないことを保証するものではありませんので、十分ご留意の上、試験結果をご利用頂けますようお願い申し上げます。
詳細はこちら
急性全身毒性試験
急性全身毒性試験
医療機器評価に関する試験で最終製品を極性/非極性の2溶媒で抽出し、2経路(静脈内投与/腹腔内投与)で投与いたします。投与後72時間まで一般症状、体重変化を観察し、観察終了時には剖検(肉眼的観察)により評価いたします。追加で血液検査、病理組織学的検査も実施可能です。
反復投与毒性試験/亜急性・亜慢性・慢性全身毒性試験
反復投与毒性試験
サンプルを臨床適用経路(経口、経皮、吸入、静脈内投与等)から一定期間反復投与し、一般症状、体重変化、摂餌量、FOB検査、尿検査、眼科学的検査を行います。投与期間は臨床適用期間を参照し各種ガイドラインに沿って設定いたします。観察終了時には剖検(肉眼的観察)、血液検査、器官重量測定、病理組織学的検査で評価し、NOAEL(無毒性量)またはNOEL(無影響量)を求めます。追加で回復期間を設け、見られた影響の可逆性の有無を確認することも可能です。化学物質・農薬などでよく用いられている「OECDガイドライン」や医療機器の「生物学的安全性評価の考え方」では指定された投与経路や期間もあります。
亜急性・亜慢性・慢性全身毒性試験
医療機器(最終製品または原材料)から抽出した試験液を反復投与し、亜急性/亜慢性全身毒性を有する物質が存在しないことを確認する試験です。標準は生理食塩液から抽出した試験液を雌雄ラットに静脈内反復投与を行いますが、臨床適用期間・用途などにより投与経路・期間(試験種)を決定いたします。検査項目として一般症状、体重変化、剖検(肉眼的観察)、血液検査、器官重量測定、病理組織学的検査を行い、対照液群と比較して評価いたします。
局所刺激性試験
皮膚一次刺激性試験/急性皮膚刺激性試験・腐食性試験
皮膚一次刺激性試験
皮膚に被験物質が接触した場合の刺激性を確認する試験です。ウサギ(またはモルモット)の健常皮膚と損傷皮膚に24時間閉塞貼付し、除去後1(または3)、24、48時間後に肉眼判定を行います。医療機器では極性/非極性の2溶媒を用いて抽出した試験液について対照液と比較して評価します。
‐試験日程例-

急性皮膚刺激性試験・腐食性試験(皮膚刺激性試験)
皮膚に被験物質が接触した場合の刺激性を確認する試験です。ウサギ(またはモルモット)の健常皮膚と損傷皮膚に24時間閉塞貼付し、除去後1(または3)、24、48時間後に肉眼判定を行います。医療機器では極性/非極性の2溶媒を用いて抽出した試験液について対照液と比較して評価します。
皮内反応試験
試験試料から抽出した試験液を皮内投与し、組織障害性や炎症誘発性の有無を確認する試験です。主に医療機器で実施されます。極性/非極性の2溶媒を用いた試験液について投与後24、48、72時間後に肉眼判定を行い、対照液と比較して評価します。ウサギ(またはモルモット)の健常皮膚と損傷皮膚に24時間閉塞貼付し、除去後1(または3)、24、48時間後に肉眼判定を行います。医療機器では極性/非極性の2溶媒を用いて抽出した試験液について対照液と比較して評価します。
連続皮膚刺激性試験
被験物質が皮膚に連続して接触した場合の刺激性を確認する試験です。ウサギ(またはモルモット)に1日1回(または数回)14日間連続で開放塗布を行い、肉眼判定により評価いたします。
‐試験日程例-
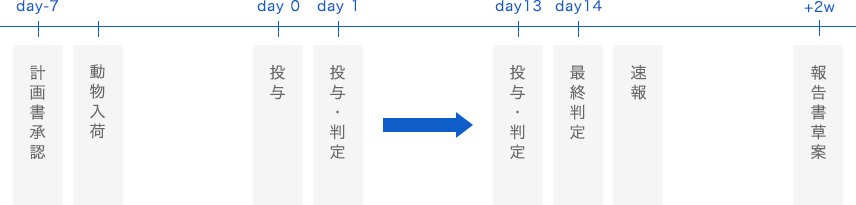
眼刺激性試験/急性眼刺激性試験・腐食性試験
被験物質が眼に接触した場合の刺激性を確認する試験です。ウサギの眼瞼結膜嚢内に1回(または数回)投与を行い、72または96時間後まで1日1回肉眼判定により評価いたします。最終判定時に刺激が残存した場合は最大21日後まで観察を延長いたします。OECDガイドラインTG405に従い、局所麻酔剤および鎮痛剤を使用し、動物に可能な限り苦痛を与えないよう配慮して行います。
‐試験日程例-

口腔粘膜刺激性試験(単回・連続)
歯科用材料・オーラルケア用品など、臨床適用経路が口腔内である場合に口腔粘膜に対する刺激性を確認する試験です。ISO 10993に従い、ハムスターの頬袋内に単回または連続投与し、観察終了後に病理組織学的検査を行い評価します。投与回数は臨床適用方法を参考にして設定いたします。医薬部外品では旧CTFAガイドラインを参照したモルモットにおける試験も実施可能です。
膣粘膜刺激性試験
膣粘膜に対する刺激性を確認する試験です。ISO 10993に従い、ウサギの膣内に1日1回5日間連続投与し、観察終了後に剖検(肉眼判定)および病理組織学的検査を行い評価します。
光毒性試験
皮膚に1回塗布後、紫外線を照射し刺激性反応の有無を確認する試験です。当社ではモルモットを使用したMorikawa法を受託しております。
‐試験日程例-

感作性試験/抗原性試験
皮膚感作性試験(感作性試験)
被験物質が皮膚に接触した場合に遅延型アレルギーを起こす可能性があるかどうかを確認する試験です。様々な試験法がありますが、各ガイドラインで推奨された方法を選択し実施いたします。
Guinea Pig Maximization Test(GPMT法)
免疫増強剤であるFreund’s Complete Adjuvant (FCA)を使用し、一般的に感度が高いと言われている試験です。OECD TG406に収載されている化学物質をはじめ、農薬、医療機器、医薬部外品・化粧品などの様々なガイドラインで第一選択として実施されている方法です。
‐試験日程例-
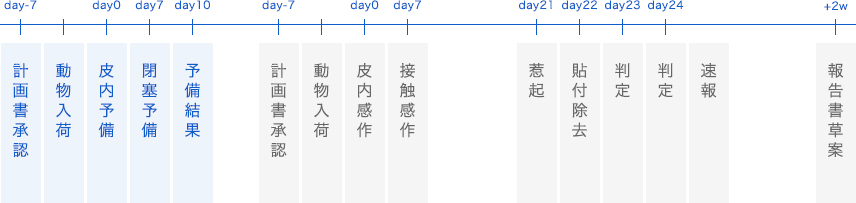
Adjuvant and Patch Test(APT法)
GPMT法と同様にFCAで処置したモルモットを使用しますが、GPMT法の「皮内感作」が難しい性状の被験物質などで選択されます。医療機器、医薬品、医薬部外品・化粧品などのガイドライン下で実施されている方法です。
Buehler Test(Buehler法)
モルモットに6時間閉塞貼付による感作を3回(または9回)行い、初回感作から28日後(または35日後)に惹起します。FCAを使用しない試験のため、GPMT法やAPT法よりも感度は低くなります。そのためOECD TG406では動物数を増やして実施するよう定められております。
Open Epicutaneous Test(OET法)
モルモットに21日間連続開放塗布にて感作し、初回感作から35日後に開放塗布惹起します。FCAを使用しない試験ですが、化粧品など毎日塗布することを目的とした被験物質では、実使用状況に近い方法として選択される場合もあります。
光感作性試験
Adjuvant and Strip Test(A&S法)
FCAを使用し、5日間連続で被験物質を開放塗布後、紫外線を照射して感作します。初回感作から21日後に開放塗布+紫外線照射により惹起し、非照射部位および対照群との皮膚反応の差より評価します。
‐試験日程例-

Harber法
FCAを用いないモルモットの試験です。感作にはUVAとUVB、惹起にはUVAを用いて行います。
抗原性試験(ASA, PCA)
能動的全身性アナフィラキシー試験(ASA)
即時型アレルギーの有無を評価する試験法です。日本薬局方・デキストラン40のモルモットを使用した試験法を始め、被験物質の臨床適用経路や使用頻度などを考慮して試験を実施いたします。
受動的皮膚アナフィラキシー試験(PCA)
ASAや各種皮膚感作性試験を行った動物から採取した血清を用い、被験物質に対する抗体の存在を確認します。モルモットに血清を皮内投与し、エバンスブルーを添加した被験物質を静脈内投与し、皮内投与部位に漏出する青色色素斑により評価します。
細胞毒性試験
細胞毒性試験では主に培養細胞を用いて、化学物質や物理作用の影響を受けた細胞のコロニー形成能や無処理群に対する細胞の生存率または死亡率により評価します。医療機器では必須の試験であり、 当社は「医療機器GLP」にも適合確認を受けています。現在、最も感受性が高いとされているV79細胞を用いるコロニー形成法をはじめ、下記試験法を受託しています。
コロニー形成による判定
- 抽出法
- 直接接触法
- 間接接触法(TCインサート法)
生死細胞による判定
- ニュートラルレッド毒性試験法
- テトラゾリウム塩を用いた毒性試験法(WST-8法)
- 遊離LDH法
発熱性物質試験
発熱性物質試験は、微生物由来の発熱性物質による汚染および発熱反応を起こすような溶出物の存在の確認を行う試験です。被験物質またはその抽出液等の試験液をウサギの静脈に投与し、発熱性物質の有無を確認します。各試験法により判定基準などが異なりますので詳細はお問い合わせください。
- 日本薬局方(JP) 4.04 発熱性物質試験法
- 米国薬局方(USP) 151
溶血毒性試験
溶血毒性試験は血液に接触する可能性の高い医療機器または材料の溶血性を評価するための試験法で,当社では医療機器の試験ガイドラインに従ったウサギの脱繊維血を用いた試験法およびASTM F756, Standard Practice for Assessment of Hemolytic Properties of Materialsに従った抗凝固血を用いた試験法も受託しております。
その他
血液学・生化学的検査や病理標本作製・病理学的検査も実施しております。詳しくはお問い合わせください。
